- CYANURE D’HYDROGÈNE
- CYANURE D’HYDROGÈNECYANURE D’HYDROGÈNEH—C 令Masse moléculaire: 27,016 gPoint d’ébullition: 26 0CPoint de congélation: — 13,24 0CDensité (à 15 0C): 0,697.Également appelé formonitrile, le cyanure d’hydrogène est un liquide incolore, très mobile, de forte odeur d’amandes amères, fortement toxique; miscible à l’eau en toutes proportions, ses solutions sont connues sous le nom d’acide cyanhydrique ou acide prussique (nom provenant du bleu de Prusse, ou bleu de Berlin).Il a été découvert par C. W. Scheele, qui l’a préparé à partir du bleu de Prusse (ferrocyanure ferrique) par action d’acide sulfurique:
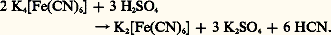 On peut aussi le préparer par décomposition de ses sels par les acides:
On peut aussi le préparer par décomposition de ses sels par les acides: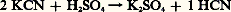 ou par oxydation catalytique d’un mélange de méthane et d’ammoniac par l’air à 1 000 0C sur toile de platine.L’acide cyanhydrique est un acide faible décomposable par l’eau. Par ébullition de ses solutions aqueuses, il se polymérise avec formation simultanée de formiate d’ammonium. Par neutralisation avec les bases, il donne des cyanures qui s’hydrolysent facilement et possèdent la même odeur que l’acide.Les cyanures alcalins trouvent beaucoup d’applications dans l’extraction et dans la concentration des minerais, ainsi que dans les procédés électrolytiques; ils sont également utilisés dans de nombreuses synthèses organiques et dans le traitement de l’acier.Les cyanures sont des poisons très puissants, car ils inhibent les processus d’oxydation cellulaire au niveau de la cytochrome oxydase. En effet, ce sont des complexants des métaux des enzymes respiratoires. Pour l’homme, la dose mortelle est de 50 milligrammes. Des doses plus faibles entraînent des vomissements, des troubles de la respiration et une perte de conscience.
ou par oxydation catalytique d’un mélange de méthane et d’ammoniac par l’air à 1 000 0C sur toile de platine.L’acide cyanhydrique est un acide faible décomposable par l’eau. Par ébullition de ses solutions aqueuses, il se polymérise avec formation simultanée de formiate d’ammonium. Par neutralisation avec les bases, il donne des cyanures qui s’hydrolysent facilement et possèdent la même odeur que l’acide.Les cyanures alcalins trouvent beaucoup d’applications dans l’extraction et dans la concentration des minerais, ainsi que dans les procédés électrolytiques; ils sont également utilisés dans de nombreuses synthèses organiques et dans le traitement de l’acier.Les cyanures sont des poisons très puissants, car ils inhibent les processus d’oxydation cellulaire au niveau de la cytochrome oxydase. En effet, ce sont des complexants des métaux des enzymes respiratoires. Pour l’homme, la dose mortelle est de 50 milligrammes. Des doses plus faibles entraînent des vomissements, des troubles de la respiration et une perte de conscience.
Encyclopédie Universelle. 2012.
